肝脏顶刊HEPATOLOGY研究成果发布!赛陆空间组学破解HBV感染核心机制
摘要:乙肝病毒感染全球近2.57亿人,可导致慢性肝炎、肝硬化、肝衰竭和肝癌。其难治性主要源于病毒cccDNA在肝细胞核内形成稳定储存库,现有治疗难以彻底清除,且病毒整合到宿主基因组可持续产生表面抗原。近期,复旦大学附属华山医院团队联合深圳市第三人民医院、赛陆等单位,在肝脏病学顶级期刊Hepatology上发表了最新研究成果。该研究开发了一种名为B-BEST的新型单细胞测序技术,可同时检测病毒复制状态和宿主转录组,首次在单细胞层面揭示HBV感染肝细胞的异质性,并发现肝细胞增殖可通过“稀释效应”减少病毒储备,为功能性治愈乙肝提供了新策略。同时,本研究依托赛陆空间转录组技术,对肝穿刺样本中的宿主转录组和病毒RNA实现1微米分辨率的原位共捕获,高精度解析肝脏组织微环境,为阐明乙肝病毒空间分布与免疫逃逸机制提供关键技术支撑。
全球约2.57亿慢性HBV感染者,乙肝功能性治愈仍是临床亟待攻克的巨大挑战。慢性HBV感染如同一个“暗箱”,传统研究依赖血液检测或整体组织分析,无法看清病毒在肝细胞中的具体分布与活动——哪些是病毒复制“工厂”、哪些是潜伏“仓库”、感染如何扰动肝脏免疫微环境?这些问题长期困扰学界。
单细胞测序技术的发展,为单细胞分辨率下解析病毒与宿主的相互作用提供了可能。然而,传统的单细胞RNA测序主要依赖oligo(dT)捕获带PolyA尾的mRNA。由于宿主mRNA背景极其强大,病毒RNA(尤其是低拷贝数的病毒RNA)难以被有效捕获,导致漏检率较高,且无法有效区分病毒的不同复制状态。这一问题已成为限制乙肝研究深入发展的关键技术痛点。
为解决这一难题,研究者创新开发了B-BEST(HBV can BE Seen on host Transcriptome)技术。其核心是在常规单细胞测序的磁珠上,巧妙加入5条HBV特异性探针,对单个细胞的全宿主转录组和病毒的五个特异性基因组区域进行超高灵敏度定量。同时,研究团队采用单细胞转录组+空间转录组联合策略,借助赛陆自主研发的高分辨率空间芯片,对肝脏组织进行深入的微环境画像分析。
研究团队开发了B-BEST技术(见图1),该技术在传统的PolyT磁珠上,创新性引入5种HBV特异性探针,分别针对HBV基因组的S区、X区、pgRNA、rcDNA和cccDNA。这一设计带来质的飞跃,相比传统方法,病毒Reads富集效率提高了100倍以上,解决了低丰度病毒RNA难以捕获的难题。同时,B-BEST能够精准区分病毒是处于活跃复制状态(pgRNA+, rcDNA+)还是整合状态(仅S/X+),实现了对病毒生命周期的单细胞级分辨率观测。B-BEST技术不仅是一个检测工具的升级,更为解析HBV生物学行为提供了强力手段。它成功摒弃了传统方法漏检的缺陷,在简化分析难度的同时,获得了真实、全面的病毒-宿主互作数据。
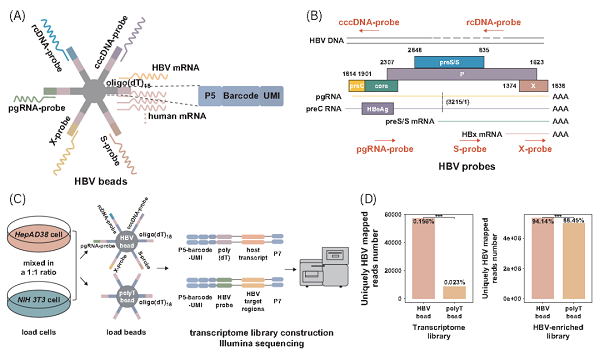
图1 B-BEST技术示意图
通过B-BEST技术,研究者对慢性乙肝患者、肝衰竭患者及治疗后的样本进行了深入分析。研究发现,HBV并非随机感染肝细胞,而是偏好特定的细胞亚群。Hep_HP亚群(高表达合成/代谢基因)和Hep_MT亚群(高表达线粒体基因)成为了HBV复制的特权生态位。这类细胞代谢活跃,病毒载量显著高于其他细胞,揭示了病毒复制对宿主代谢机制的依赖。而在未治疗的慢性乙肝患者中,只有不到15%的感染细胞激活了干扰素刺激基因。这表明HBV极善于免疫逃逸,大部分感染细胞处于隐身状态,逃逸了免疫系统的监视。此外,研究利用人源化肝脏小鼠模型,比较了恩替卡韦(ETV)和聚乙二醇干扰素的治疗效果,发现当病毒复制被抑制后,肝细胞的增殖(克隆扩增)会稀释细胞内的病毒库。这提示功能性治愈可能部分得益于健康肝细胞的再生替代了感染细胞。
这项研究不仅绘制了HBV感染的单细胞全景图谱,更具有深远的临床指导意义。随着对HBV感染机制研究的深入,先进检测工具的重要性日益凸显。B-BEST技术凭借其卓越的灵敏度和精准的分型能力,将成为病毒学研究领域的利器。未来,随着多组学技术的迭代,B-BEST将持续助力科研人员探索生命奥秘,为终结乙肝威胁提供更精准的科学支撑。
单细胞技术需将组织消化成悬液,会丢失所有空间位置信息。那B-BEST的发现是真实的空间规律吗?这篇发在Hepatology的研究采用了空间组学的方法来进行验证(见图2)。研究团队选用了赛陆自主研发的高分辨率空间芯片,通过赛陆自主开发的空间组学分析软件给出了答案。
利用赛陆空间转录组芯片,研究团队成功构建了高精度的肝脏组织空间图谱。赛陆芯片的高捕获效率和优异灵敏度,确保在复杂肝脏组织背景下,能够精准捕获低丰度的病毒RNA信号。这不仅保留了肝细胞、免疫细胞的空间位置信息,更直观展示了病毒感染区域与免疫浸润区域的相互关系。结合单细胞数据,研究发现HBV并非随机感染,而是偏好特定的代谢活跃区域。通过SalusSTS®软件的空间聚类与共定位分析,研究人员精准锁定了病毒复制的特权生态位。这些发现揭示了病毒如何利用宿主代谢机制进行复制,以及如何在空间上规避免疫系统的监视。在治疗机制的研究中,空间组学技术同样发挥了不可替代的作用。研究显示,当病毒复制被抑制后,肝细胞的增殖会稀释细胞内的病毒库。空间组学数据进一步证实,新生的健康肝细胞在空间上逐步替代了感染细胞,这一增殖稀释效应的发现,为临床实现功能性治愈提供了直观的空间证据。
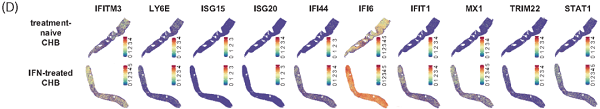
图2 肝穿刺样本空转基因表达热图
本研究能够发表在Hepatology这一顶级期刊,离不开扎实的数据质量与深度生物学解析,赛陆空间组学展现了在深度解析上全方位的技术优势。赛陆空间组学芯片采用了创新的捕获技术,具有极高的信噪比,可高效捕获低拷贝病毒RNA,确保了数据的完整性与真实性。而赛陆配套的空间组学分析软件,提供了从基础聚类、细胞通讯到高级共定位分析的全流程解决方案,高效完成病毒-宿主相互作用的空间映射,大幅缩短了从数据到发现的周期。本研究展示了赛陆在多组学联合分析方面的成熟经验。从单细胞到空间转录组,赛陆提供了一站式的技术支持,帮助科研团队打通了微观分子与宏观组织结构之间的壁垒。
本研究不仅绘制了HBV感染的单细胞与空间全景图谱,更展示了赛陆空间组学技术在感染性疾病研究中的巨大潜力。凭借其高灵敏度、高分辨率及强大的分析软件,赛陆空间转录组解决方案可助力研究人员在肿瘤微环境、感染免疫、组织发育等领域获得更精准的生物学发现。未来,赛陆将继续深耕空间组学技术,以硬核产品助力科学家探索生命奥秘,让每一次实验都更有价值。
国产优选测序方案
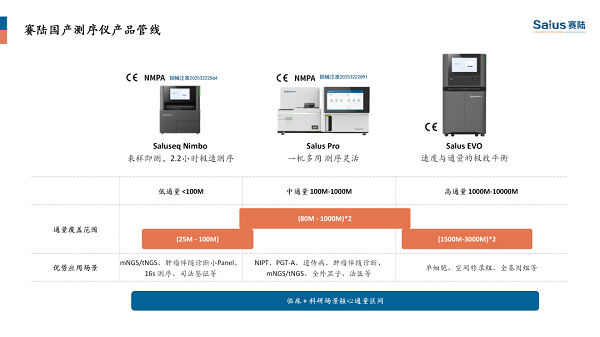
关于赛陆
赛陆创办于2020年,是国家高新技术企业和国家专精特新小巨人企业,专注于开发自主知识产权的上游测序平台、超分辨空间组学平台和固相基因芯片检测平台,实现基因组学、空间组学以及基因芯片产品的自主开发及科研临床端转化。公司突破了以往测序和组学产品在通量、成本、分辨率、自动化等方面的瓶颈,取得国家药监局NMPA三类医疗器械注册证、欧盟CE-IVDR等多项关键认证。公司发展迅速,现拥有国际领先的测序、组学和芯片平台,可以为中下游应用提供全面的解决方案,产品畅销海内外。



















